Capítulo 4 Biosfera
4.1 Introdução
O termo biosfera foi empregado pela primeira vez em 1875 pelo geólogo austríaco Eduard Suess. Ele representa a soma de duas expressões vindas do grego: βίος (bíos) que significa vida e σφαίρα (sfaira) que significa esfera. Em outras palavras, a biosfera corresponde ao espaço em que há vida na Terra, ou seja, ao universo dos organismos vivos e suas interações. Esse termo trata de diversos tópicos químicos e biológicos que afetam diretamente a saúde humana e a ecológica, com destaque para a produção de alimento, nutrição, substâncias tóxicas e pesticidas. Em comum, está a necessidade de que os organismos vivos tenham de absorver e processar materiais do mundo à sua volta.
A Biosfera correlaciona todos os componentes abióticos do nosso planeta e que podem ser representados pelos oceanos, mares, lagos e rios, que ocupam 3/4 da Terra e que correspondem à Hidrosfera; assim como o espaço formado por solo e uma grande variedade de rochas que em sua maioria está coberta por solo e outros depósitos de sedimentação correspondem à Litosfera; e por fim, o espaço formado por gás que corresponde à Atmosfera. O conjunto desses componentes com os seres vivos é que forma a Biosfera.
Como podemos observar na Figura 4.1, o limite superior da Biosfera está em torno de 7.000 metros e seu limite inferior em 11.000 metros, totalizando uma faixa de, aproximadamente, 18.000 metros. A maioria dos seres vivos terrestres encontra-se em até 5.000 metros acima do nível do mar e nos oceanos, contudo, algumas bactérias, já foram encontradas a mais de 9.000 metros de profundidade, mas a maioria está a até 150 m de profundidade.
A diversidade de características que existe nesses ambientes se traduz na diversidade de espécies e na quantidade de seres vivos que habitam determinadas regiões. Assim, nos extremos superior e inferior da biosfera, poucos seres vivos conseguem viver. As condições ambientais mais favoráveis estão nos limites intermediários dessa faixa. Devido à essa interação entre seres vivos e biótopo da biosfera, percebemos que essa camada de nosso planeta é modificada a todo tempo, tornando-se um espaço heterogêneo.
Por meio da atuante presença do homem no ambiente e muitas vezes de maneira transformadora, a fragilidade da Biosfera se evidencia. Entretanto, essa faixa também se mostra autorreguladora, dinâmica e capaz de resistir, ao menos dentro de certos limites, às modificações do meio ambiente.
4.2 A produção de alimentos
Para melhor compreensão dos fenômenos ambientais, é de fundamental importância imaginá-los a partir dos ciclos biogeoquímicos. Em outras palavras, essas ocorrências devem sempre ser interpretadas levando-se em consideração os importantes fluxos de matéria e energia, que ocorrem dinamicamente entre os componentes abióticos do nosso planeta. Nesse contexto, devemos em primeiro lugar, considerar a produção de alimentos e o importante papel do ciclo do nitrogênio.
Como vimos anteriormente, o principal processo envolvido na produção de energia biológica é a conversão fotossintética de CO2 em compostos de carbono reduzidos, que são posteriormente utilizados como combustível por todas as formas de vida. Além do carbono, os organismos necessitam de outros nutrientes, tais como o nitrogênio e o fósforo dentre outros elementos em quantidades menores. Esses elementos estão geralmente disponíveis no solo em quantidade suficiente para sustentar um nível adequado de crescimento natural das plantas.
Assim, podemos inferir que a possibilidade de aumento da produtividade de uma planta, além dos limites naturais, é normalmente restringida pelo suprimento de nitrogênio que ela tem à disposição. Porém, esse nitrogênio deve ser fixado, ou seja, combinado com outros elementos, para participar de reações biológicas e os quase 80% de N2 que compõem a atmosfera estão em uma forma extremamente estável e não reativa. Como vimos anteriormente, no ciclo do nitrogênio (Figura 4.4), parte do N2 é fixado de forma não biológica por meio da reação com o O2 em temperaturas suficientemente altas via combustão ou por meio de relâmpagos. Já os óxidos de nitrogênio formados na atmosfera são convertidos em ácido nítrico e lavados na chuva, fornecendo, desse modo, suprimento de nitrato ao solo. As plantas podem utilizar nitrato na produção de proteínas e outros compostos orgânicos essenciais de nitrogênio.
Entretanto, a quantidade de nitrogênio disponível por meio da rota dos óxidos de nitrogênio e nitrato é insuficiente para sustentar a abundante vida vegetal tal qual a conhecemos. A maior parte da fixação de nitrogênio que ocorre naturalmente é realizada por certas bactérias e algas azul-esverdeadas que são capazes de reduzir o N2 para NH3. Assim, as plantas podem usar amônia diretamente como fonte de nitrogênio e os animais podem obter nitrogênio ingerindo as plantas. Esse ciclo é fechado quando as plantas e os animais morrem e o nitrogênio reduzido em seus tecidos é convertido em amônia pela decomposição bacteriana e adicionado ao reservatório de amônia.
4.2.1. Fertilidade do solo e a agricultura
O conceito de fertilidade do solo também está intimamente relacionado aos vários fluxos de matéria e energia no ambiente. Assim, as principais fontes naturais de nitrogênio para fins agrícolas são as bactérias que contêm nitrogenase, algumas das quais crescem em simbiose com uma limitada variedade de plantas cultivadas, mais notadamente aquelas da família das leguminosas. A capacidade de fertilização das leguminosas é a razão para a rotação de cultivos.
A rotação de cultivos é uma antiga prática agrícola em que as leguminosas são plantadas de forma alternada com os cereais, grãos e outros vegetais para manter a produtividade das plantas.
Na ausência da rotação de culturas, as plantas que não fixam nitrogênio esgotam rapidamente os depósitos de nitrogênio no solo, a menos que esses sejam reabastecidos pela adição de adubos e fertilizantes.
Em 1840, o químico alemão Justus Von Liebig observou a relação entre o crescimento de plantas e a utilização de fezes de animais como adubo. Desde então, a adubação tem sido utilizada no manejo de solos como uma forma de atender à demanda cada vez maior por alimentos.
Nas últimas décadas, os fertilizantes naturais têm sido substituídos por fertilizantes artificiais produzidos industrialmente. Como já mencionado, a produção industrial de fertilizantes de nitrogênio é realizada por meio do processo de Haber-Bosch e corresponde ao dobro da taxa estimada de fixação de N2 de culturas leguminosas.
A aplicação de fertilizantes pode melhorar consideravelmente a produção agrícola. Um exemplo disso é a quase quadruplicação da produção de milho e outros grãos nos Estados Unidos e no meio oeste canadense entre 1950 e 2000. Além disso, a produção agrícola aumentou em toda parte por decorrência da disponibilidade de fertilizantes e do aprimoramento das linhagens das culturas.
A melhoria na produção foi particularmente importante para os países pobres, muitos dos quais fizeram grande progresso na expansão da produção agrícola para atender às necessidades nutricionais das populações em crescimento. Muito se realizou na década de 1960 por meio da chamada “Revolução Verde”, quando cientistas de institutos de pesquisa no México e nas Filipinas desenvolveram novas linhagens de trigo e arroz altamente produtivas quando fertilizadas.
Contudo, a adubação sem acompanhamento técnico agrícola, planejamento de culturas de acordo com a topografia da propriedade e conhecimento prévio do tipo de solo tem causado vários impactos ambientais e prejuízos financeiros ao agricultor. Além de salinizar o solo, a aplicação de fertilizante pode causar a eutrofização de mananciais devido à lixiviação de fertilizantes aplicados em solos revolvidos que ocorre, sobretudo, em épocas de chuvas.
Outro fator importante em relação à melhoria da produção agrícola é a irrigação. Essa técnica já era usada na antiguidade, mesmo sem o conhecimento prévio dos efeitos dos fluxos de energia e matéria entre os reservatórios. O que se tinha era apenas um senso comum de que a disponibilidade de água no solo estava diretamente relacionada à sua produtividade. Hoje em dia, essa produtividade é atribuída às características que tem a água de atuar como veículo de transporte e na dissolução de nutrientes para as plantas. A intensidade da acumulação de sais no solo depende da qualidade da água de irrigação, do manejo e da eficiência da drenagem.
Em solos em que há escassez de água, como no nordeste brasileiro e em alguns países árabes, é comum a utilização da irrigação mecânica, que consiste na captação de mananciais utilizando bombas e distribuindo-os nas lavouras.
4.3 Pesticidas
Se existe um sentido mais adequado para a expressão “mal necessário” esse pode ser evidenciado no uso de pesticidas pela agricultura moderna. Apesar de toda a toxicidade que esses compostos apresentam e que será bem destacada nessa seção, a grande explosão demográfica que a humanidade vivenciou no último século e que está diretamente atrelada ao crescimento exponencial da demanda alimentícia, só foi possível devido ao uso de pesticidas pela agricultura. Em outras palavras, os pesticidas surgiram como uma saída para garantir a elevada produção agrícola e o suprimento da demanda por alimentos. Hoje em dia, é impossível imaginar a produção de alimentos sem o uso desses compostos, pois esses viabilizam a produção agrícola, garantindo a diminuição dos preços dos alimentos e da mão de obra.
Por definição os pesticidas são todas as substâncias de origem natural ou sintética utilizadas no controle e/ou eliminação de pragas (insetos, ervas daninhas etc.), que causam prejuízos na produção de alimentos ou transferem enfermidades aos seres humanos.
Como veremos a seguir, os pesticidas atuam interagindo no metabolismo vital dos organismos vivos aos quais se destinam.
Atualmente, a maior parte de todas as culturas de alimentos comercializados é produzida com o uso de pesticidas sintéticos, exceto em fazendas de cultivo de produtos orgânicos, em que são usados os pesticidas naturais. A Tabela 4.1 apresenta as várias categorias de pesticidas e seus principais alvos.
Todavia, desde a sua introdução, os pesticidas sintéticos têm sido um problema para a saúde humana, devido à potencial contaminação dos alimentos proporcionada por esses compostos. Para exemplificar essa problemática, atualmente, metade dos alimentos consumidos nos Estados Unidos contém um nível mensurável de, no mínimo, um tipo de pesticida. Em contrapartida, outros países vêm proibindo ou restringindo o uso de alguns pesticidas mais tóxicos.
Tabela 4.1. Categoria de pesticidas e organismos indesejáveis combatidos.
| Tipo de pesticida | Organismo alvo |
|---|---|
| Acaricida | Ácaros |
| Algicida | Algas |
| Avicida | Aves |
| Bactericida | Bactérias |
| Desinfetante | Micro-organismos |
| Fungicida | Fungos |
| Herbicida | Plantas |
| Inseticida | Insetos |
| Larvicida | Larvas de insetos |
| Moluscicida | Caracóis e lesmas |
| Nematicida | Nematóides |
| Piscicida | Peixes |
| Raticida | Roedores |
| Cupicida | Cupins |
Atividade 4.1
Registre em um pequeno texto dissertativo de dez linhas, sua opinião acerca dos tópicos: pesticidas, demanda alimentícia e explosão demográfica.
4.3.1. Inseticidas tradicionais
Os inseticidas tradicionais são usados pela sociedade há séculos, principalmente no controle de doenças transmitidas por insetos ou roedores que servem de hospedeiros para diversas enfermidades (malária, febre amarela, peste bubônica etc.). Os inseticidas tradicionais também são, geralmente, empregados na prevenção de insetos que atacam as culturas de alimentos e no controle de mosquitos e moscas domésticas que são inconvenientes e proliferam doenças.
O mais antigo registro de uso de inseticidas pela humanidade data de 1000 anos a.C. e descreve a queima de enxofre por fumigação em casas na Grécia.
Fumigação é um tipo de controle de pragas por meio do tratamento químico realizado com compostos químicos ou formulações pesticidas (os chamados fumigantes) voláteis (no estado de vapor ou gás) em um sistema hermético, visando à desinfestação de materiais, objetos e instalações que não possam ser submetidas a outras formas de tratamento. Um exemplo prático é o uso de dióxido de enxofre (SO2), produzido pela queima do enxofre elementar sólido, algumas vezes por incorporação do elemento em velas, que perdurou até o século XIX.
Ao longo da história, diversos outros tipos de materiais de origem natural já foram usados como inseticidas, tais como o mercúrio, o arsênio, a nicotina e o tabaco. Contudo, tais compostos são mais tóxicos para os humanos e outros mamíferos, especialmente nas doses necessárias para serem eficazes como pesticidas. Além disso, metais e semimetais tóxicos, como os compostos com arsênio usados em pesticidas, não são biodegradáveis e permanecem indefinidamente na água e em organismos vivos, solos ou sedimentos e podem até mesmo entrar na cadeia alimentar.
4.3.2. Inseticidas organoclorados
As tentativas de combate às pragas de insetos foram relativamente ineficazes até o desenvolvimento dos inseticidas químicos modernos. O primeiro deles foi o para-diclorodifeniltricloroetano, mais conhecido pela sigla DDT (Figura 4.2) e que foi sintetizado pelos aliados durante a Segunda Guerra Mundial para controlar as epidemias de tifo e malária. Por sua descoberta, o químico suíço Paul Hermann Müller recebeu o Prêmio Nobel de Medicina em 1948.
Após a guerra, o DDT foi o primeiro pesticida de uso agrícola usado amplamente, devido às diversas características que o qualificam como inseticida ideal. Dentre essas podemos destacar:
a. elevada estabilidade química, degrada-se somente de forma lenta, sob condições ambientais;
b. baixa solubilidade em água, exceto na presença de oxigênio ou nitrogênio nas moléculas;
c. alta solubilidade em meios lipofílicos, como o tecido adiposo de seres vivos;
d. toxicidade relativamente alta para insetos, mas baixa para humanos.
Essas características fazem do DDT um inseticida persistente, ou seja, cada aplicação dura por um longo tempo.
Por ser hidrofóbico, o DDT penetra rapidamente na camada externa cerosa dos insetos e, após a penetração, paralisa-os rapidamente. Ele atua ligando-se às células nervosas de insetos mantendo abertos os canais moleculares que admitem os íons de sódio. A abertura desses canais acarreta o estímulo descontrolado dos nervos.
Entretanto, não demorou muito para os insetos ganharem resistência ao DDT, o que acarretou em sua perda de eficácia e o declínio de seu uso por volta de 1960. Em meados de 1970, o DDT foi proibido para a maioria de seus usos em diversos países industrializados.
O ganho de resistência ao DDT por parte dos insetos se deve à produção de uma enzima chamada DDT-ase, que catalisa a deidrocloração (perda de átomos de H e Cl) do DDT para formar o 2,2-bis-p-clorofenil-1,1-dicloroetileno, também conhecido como DDE, que possui uma nova ligação dupla no átomo de carbono central. A alteração da geometria desse carbono de tetraédrica para trigonal altera as características do DDT, que não se liga mais fortemente às células nervosas dos insetos.
Por isso, para complementar e substituir o DDT, novos inseticidas foram desenvolvidos. A princípio foram sintetizadas variações do DDT, ou seja, moléculas que mantêm a estrutura do DDT, mas que possuem diferentes substituintes químicos, que não são suscetíveis à DDT-ase dos insetos resistentes (Figura 4.3).
As variações mais bem sucedidas tiveram o uso disseminado, até que a resistência a essas variações também foi desenvolvida pela população de insetos. Por fim, concluiu-se que nenhum inseticida poderia permanecer eficaz por muito tempo, o que estimulou o desenvolvimento de novas versões. A partir de então outras moléculas organocloradas foram empregadas como neurotoxinas de insetos. Várias delas eram produtos de uma reação de adição entre o pentaclorociclopentadieno e uma molécula olefínica que originaram a classe dos inseticidas ciclodiênicos, com destaque para o aldrin, dieldrin, clordano e endosulfan.
Contudo, o sucesso dos inseticidas persistentes teve um preço alto em todo o ecossistema em que estavam inseridos. Isto ocorre porque os insetos fazem parte de uma rede muito complexa de relação predador-presa. Como exemplo dessa ação, temos a introdução do DDT em Bornéu, como parte de uma campanha de erradicação da malária pela Organização Mundial da Saúde, na década de 1960, quando os mosquitos realmente foram eliminados, mas também outras espécies de mosquitos, incluindo uma vespa que era predadora das lagartas que viviam nos telhados de sapé das casas da aldeia. Sem as vespas, a população de lagartas se multiplicou e os telhados de sapé foram consumidos. Além disso, os mosquitos mortos foram comidos por lagartixas, que adoeceram e se tornaram presa fácil para a população de gatos. Por terem comido as lagartixas doentes, os gatos também adoeceram e morreram, provocando multiplicação da população de ratos. Os ratos comeram as plantações locais e ameaçaram uma deflagração de peste bubônica. Para tentar minimizar os efeitos colaterais da quebra do ecossistema, o governo de Bornéu teve de reintroduzir os gatos na região afetada.
Essa correlação de fatos ilustra o princípio da bioacumulação em cadeias alimentares. Esse princípio descreve que as substâncias químicas na presa se concentram no predador, caso não sejam degradadas e expelidas rapidamente.
Existem algumas tecnologias que permitem a recuperação ou remediação de solos contaminados e/ou degradados. Tais tecnologias se baseiam nas propriedades químicas de substâncias e/ou processos físicos que serão utilizados para retenção, mobilização ou destruição de um determinado contaminante presente no solo. A mais empregada é a biorremediação, que nada mais é do que a utilização de organismos vivos, especialmente micro-organismos, para degradar ou transformar poluentes ambientais em substâncias de menor toxicidade. Outro tipo de remediação que tem se tornado uma tecnologia emergente é a fitorremediação, isto é, o uso de vegetação para a descontaminação in situ de solos e sedimentos.
Atividade 4.2
Explique a conexão mosquito-lagartixa-gato com o princípio da bioacumulação em cadeias alimentares.
4.3.3. Inseticidas organofosforados e carbamatos
Devido aos problemas ligados à bioacumulação, os inseticidas organoclorados foram amplamente substituídos por compostos altamente potentes, não persistentes e que se quebram rapidamente em produtos inofensivos e solúveis em água. Dentre esses compostos as duas classes mais usadas são os organofosforados e os carbamatos, inseticidas que são poderosas neurotoxinas e atuam inibindo a enzima acetilcolinesterase, que hidrolisa o neurotransmissor acetilcolina.
Os neurotransmissores são moléculas liberadas por uma célula nervosa para estimular outra célula nervosa adjacente. Eles se difundem através do espaço entre as células, chamados de sinapse, e se ligam a receptores na segunda célula. A acetilcolina é a molécula neurotransmissora responsável por estimular as células nervosas motoras nos organismos vivos superiores.
Quando a acetilcolina se liga aos seus receptores, uma célula nervosa motora continua a fornecer estímulo até a acetilcolina ser quebrada pela acetilcolinesterase, que está presente na sinapse. Se a acetilcolinesterase for inibida, o estímulo dos nervos continuará de forma descontrolada, levando à paralisia e à morte.
Os inseticidas organofosforados apresentam a seguinte fórmula geral (Figura 4.4):
Dentre os inseticidas organofosforados podemos destacar o paration, o malation e o clorpirifós (Figura 4.5):
Já os carbamatos apresenta a seguinte fórmula geral (Figura 4.6):
Dentre eles podemos destacar o carbaril e o aldicarb (Figura 4.7):
A toxicidade dos inseticidas organofosforados e carbamatos é bem maior do que a dos inseticidas organoclorados ao passo que os pesticidas paration e aldicarb têm causado morte e danos à saúde de muitos trabalhadores agrícolas. Tais fatos fazem com que as vantagens ambientais adquiridas por esses agentes não persistentes sejam completamente neutralizadas pelos impactos causados à saúde humana.
4.3.4. Inseticidas naturais
Muitas plantas podem produzir moléculas para sua própria proteção. Essas moléculas podem matar ou inativar insetos, o que tem despertado a atenção dos químicos que podem, por sua vez, isolar alguns desses compostos para serem empregados no controle de insetos. Os principais exemplos são a piretrina, a nicotina, a rotenona, os feromônios e os hormônios juvenis.
Há séculos o homem já vem usando a piretrina, que é extraída de flores de uma espécie de crisântemo. Na forma de inflorescências secas, as piretrinas foram usadas pelo exército napoleônico para controlar piolhos e ainda hoje são usadas na forma de aerossóis como antipulgas para animais. Seu mecanismo de ação é semelhante ao dos inseticidas organofosforados, já que paralisam os insetos embora geralmente não os matem. Contudo, esses compostos são instáveis à luz solar o que fez com que os cientistas desenvolvessem piretrinas sintéticas para uso externo.
Outro inseticida natural que merece destaque é a rotenona, um produto natural complexo derivado de raízes de feijão. Esse inseticida natural vem sendo usado em colheitas há 150 anos, e, há séculos, vem sendo usado para paralisar e/ou eliminar peixes. No entanto, esse composto também é fotossensível, além disso, há evidências epidemiológicas e toxicológicas de que a exposição crônica à rotenona pode contribuir para o mal de Parkinson.
4.3.5. Herbicidas
Nos tempos bíblicos, os exércitos usavam sal ou uma mistura de salmoura e cinzas para esterilizar alguns territórios que tinham conquistado na tentativa de torná-los inabitáveis para as gerações futuras do inimigo. Já na primeira metade do século XX vários compostos inorgânicos, tais como o arsenito de sódio (Na3AsO3), clorato de sódio (NaClO3) e sulfato de cobre (CuSO4), já eram usados para matar algumas ervas indesejáveis para a lavoura, conhecidas como ervas daninhas. Mas o que todos esses compostos tinham em comum? Todos pertencem a um grupo de pesticidas conhecidos como herbicidas.
Os herbicidas são compostos químicos que destroem plantas. Eles são empregados na agricultura comercial para substituir a extração manual e mecânica de ervas daninhas sem causar prejuízos à vegetação desejável. Além de poupar mão de obra, os herbicidas são aplicados no plantio direto, minimizando a erosão por reduzir a perturbação do solo.
No plantio direto, os campos são plantados sem ser arados, injetando diretamente as sementes no solo após as ervas daninhas terem sido controladas com herbicidas.
O plantio direto exige altos níveis de herbicidas, pois as ervas daninhas devem ser completamente erradicadas, uma vez que uma pequena porcentagem das ervas remanescentes produz sementes suficientes para restaurar a população de ervas e obstruir a plantação.
Assim como ocorreu com os pesticidas, o uso de herbicidas caiu a partir da década de 1980, em parte devido às preocupações decorrentes dos efeitos colaterais contra a saúde e o ecossistema.
Os herbicidas podem ser agrupados por atividade, por uso, por modo de ação, por grupo químico ou por tipo de vegetação controlada. Quanto à atividade eles podem ser classificados como herbicidas de contato ou como herbicidas sistêmicos. Quanto ao uso, eles podem ser classificados em herbicidas aplicados no solo, em pré-emergentes e em pós-emergentes. Quanto ao mecanismo de ação ou etapa bioquímica afetados na planta eles podem ser classificados em herbicidas inibidores da acetil-coenzima A-carboxilase, em herbicidas inibidores da acetolactato-sintase, em herbicidas inibidores da enolpiruvil-shikimato 3-fosfato-sintase, auxina sintética e em herbicidas inibidores do fotossistema.
A maior classe de herbicidas é a das triazinas, das quais a mais conhecida é a atrazina (Figura 4.8) que é o principal agente usado nas plantações de milho.
A atrazina não se bioacumula de forma significativa, sendo moderadamente solúvel em água, contudo é bastante persistente e frequentemente detectável em poços de fazenda. Embora não seja muito tóxica, há certa correlação entre as altas concentrações de atrazina em poços artesianos, o câncer e a má-formação fetal. Tais eventos fazem com que a atrazina venha sendo substituída em algumas regiões pelo herbicida metolaclor, que se degrada mais rapidamente no campo.
Outro herbicida muito comum é o paraquat (Figura 4.9) que tem sido usado extensivamente em campanhas de erradicação da maconha. Contudo, é altamente tóxico e pode provocar danos pulmonares a alguns fumantes de maconha. Por isso, o paraquat tem seu uso restrito em muitos países do mundo, considerando seu potencial significativo para intoxicações acidental ou intencional. Nas últimas décadas, o paraquat foi um agente bastante popular para o suicídio, mas, atualmente há declínio do envenenamento intencional. Ele se apresenta em soluções a 20% e tem propriedades tóxicas complexas.
O paraquat é altamente tóxico ao homem por ingestão; seu efeito tóxico em mamíferos é, em grande parte, devido ao dano para os alvéolos pulmonares. É bem absorvido por via digestiva e moderadamente pela pele irritada ou lesada, mas, não é absorvido significativamente pela pele intacta. É altamente irritante para os olhos, contudo, a via inalatória tem menor absorção. A absorção de névoa de spray pode acontecer, mas não parece ser de significado prático. Devido à alta letalidade do paraquat, houve associação de um emético em sua formulação, na tentativa de reduzir a absorção na ingestão acidental ou intencional.
Como podemos observar na Figura 4.10, está bem estabelecido que o “Ciclo Redox” é a reação primária responsável pela toxicidade do paraquat. Em condições anaeróbicas, o cátion paraquat pode ser reduzido por meio de NADPH microssomal dependente para formar o radical reduzido. Esse, então, reage com oxigênio molecular para formar o cátion de paraquat e o íon superóxido. O paraquat continuará então o ciclo de oxidação para a forma reduzida com os elétrons do oxigênio, causando morte celular por lipoperoxidação das membranas celulares ou depleção de NADPH, como no pulmão, em que há acumulação seletiva tanto nos pneumócitos tipo I e II.
Por fim, outro herbicida que merece destaque é o pentaclorofenol ou simplesmente PCF (Figura 4.11), que se apresenta como um sólido branco com odor fenólico, insolúvel em água, mas que dissolve rapidamente em óleos e gorduras. Normalmente é encontrado na forma de sal, principalmente o pentaclorofenato de sódio e pode conter dioxinas (por exemplo, tetra-, hexa- e octaclorodibenzo-p-dioxina) e hexaclorobenzeno como subprodutos de fabricação. Ele é usado como conservante de madeira, desfolhante na cultura de algodão, herbicida pré-emergente e biocida em sistemas de água. Atualmente seu uso está proibido em muitos países, inclusive no Brasil.
Contudo, o pentaclorofenol ainda pode ser encontrado no ar (na forma de vapor), em águas superficiais e subterrâneas (na forma de sal ionizado) ou adsorvido a solos e sedimentos. A contaminação atmosférica pode ocorrer por volatilização da madeira tratada e resíduos das fábricas de tratamento da madeira. O PCF também pode ser formado durante a incineração de resíduos contendo cloro. O composto pode atingir corpos d'água, persistindo por bastante tempo, e contaminar solos e sedimentos.
O PCF pode estar presente em peixes e outros organismos devido à alta solubilidade do sal sódico em água, mas os níveis nos tecidos geralmente são baixos. Alimentos acondicionados em caixas de madeira tratada com PCF também podem ser contaminados.
A exposição por inalação de ar ou ingestão de água potável e de alimentos contaminados com PCF é pouco significativa, mas aumenta em regiões próximas a fábricas que utilizam o composto ou em locais de despejo de efluentes dessas empresas. Os maiores níveis ocorrem na exposição ocupacional, principalmente por inalação e contato dérmico, em fábricas de tratamento de madeira ou em plantações que usam o agrotóxico. Essa exposição pode resultar em concentrações de PCF, no sangue e na urina dos trabalhadores, duas vezes maiores do que na população não exposta. A inalação de pentaclorofenol provoca irritação no trato respiratório, garganta e olhos, produzindo sensação de queimação e lacrimejamento. Na exposição a altas doses pode ocorrer febre alta, fraqueza, alterações respiratórias, pressão sanguínea, convulsão e colapso. A exposição crônica a pequenas quantidades pode causar danos aos rins, fígado e sistema nervoso e alterações hematológicas.
Estudos com animais indicam que o PCF causa efeitos fetotóxicos e embriotóxicos, e que o composto se une a vários receptores hormonais. Evidências epidemiológicas sugerem abortos espontâneos, redução do peso ao nascer e outras más-formações.
Porém, nem todos os herbicidas devem ter seu uso banido, em virtude de seus efeitos colaterais. Um exemplo positivo foi o desenvolvimento de herbicidas de baixa toxicidade e que se degradam prontamente no meio ambiente. O mais conhecido deles é o glifosato (Figura 4.12), um simples derivado de aminoácidos, solúvel em água, mas que adere bem ao solo.
Em virtude de sua estrutura iônica, o glifosato é atraído aos locais de troca iônica nas partículas do solo, não sendo, portanto, carregado para o lençol freático. Além disso, por ser metabolizado pelos micro-organismos do solo, o glifosato possui uma meia-vida de apenas 60 dias, não se bioacumulando em proporções significativas.
O mecanismo de ação do glifosato parte da inibição de uma enzima presente na folha e que é necessária para a síntese dos aminoácidos aromáticos fenilalanina, tirosina e triptofano. O bloqueio desse caminho biossintético essencial mata a planta. Já os animais não são afetados pelo glifosato, uma vez que eles o eliminam rapidamente.
4.4 Alimentos geneticamente modificados
Um tópico que merece destaque especial quando se trata de aumento da produção agrícola é o uso de organismos geneticamente modificados para essa finalidade. Isso só é possível devido à contínua revolução na genética molecular que viabilizou a reprogramação das instruções genéticas das plantas. Os cientistas decifraram o código genético das moléculas de DNA durante a década de 1950 e gradualmente elucidaram os complexos mecanismos bioquímicos por meio dos quais os genes se expressam. Por isso, eles aprenderam a isolar os genes e a recombiná-los como um complemento do DNA do organismo (o genoma). A partir de todas essas descobertas científicas foi possível o desenvolvimento da indústria da biotecnologia.
A engenharia genética foi primeiramente desenvolvida para as bactérias e depois para as levedura e culturas de células de organismos superiores. Essa técnica permitiu à indústria farmacêutica fabricar proteínas cruciais à medicina, tais como a insulina e o hormônio do crescimento, ao inserir gene em bactérias ou em outras células, e colher o produto.
Os cientistas também aprenderam a inserir genes estranhos no genoma de uma planta e a produzir sementes que contêm novas características. Esse trabalho deu origem, em meados de 1995, às primeiras culturas comerciais geneticamente modificadas ou transgênicas como são popularmente conhecidas, sendo amplamente adotada nos anos subsequentes. Apesar da resistência aos alimentos transgênicos nos mercados europeus, já em 1999, cerca de 40 milhões de hectares de culturas geneticamente modificadas já haviam sido plantadas no mundo, abrangendo metade do cultivo de soja nos Estados Unidos e mais de um terço do milho.
A modificação genética das plantas ocorre em várias fases:
1. inicialmente, o cientista encontra e isola o gene com as características genéticas desejadas, processo denominado de mapeamento;
2. em seguida, faz várias cópias do gene isolado num processo designado PCR (reação em cadeia da polimerase);
3. no próximo passo, o cientista transfere os genes desejados para os genes das próprias plantas (utilizando um pedaço de tecido da planta). Para inserir os genes desejados na planta, o cientista tem 3 opções: pode utilizar um "canhão de genes", uma bactéria do solo ou um material chamado protoplasto. Os métodos de inserção de genes são chamados de transformação;
4. em seguida, o cientista cria uma nova planta a partir do tecido da planta geneticamente modificada;
5. verifica se os genes inseridos funcionam conforme esperado;
6. por fim, verifica também se o gene inserido aparece nas sementes.
Para exemplificar todas essas etapas a Figura 4.13 apresenta um esquema da transformação genética de uma planta por meio de uma bactéria e de um plasmídeo.
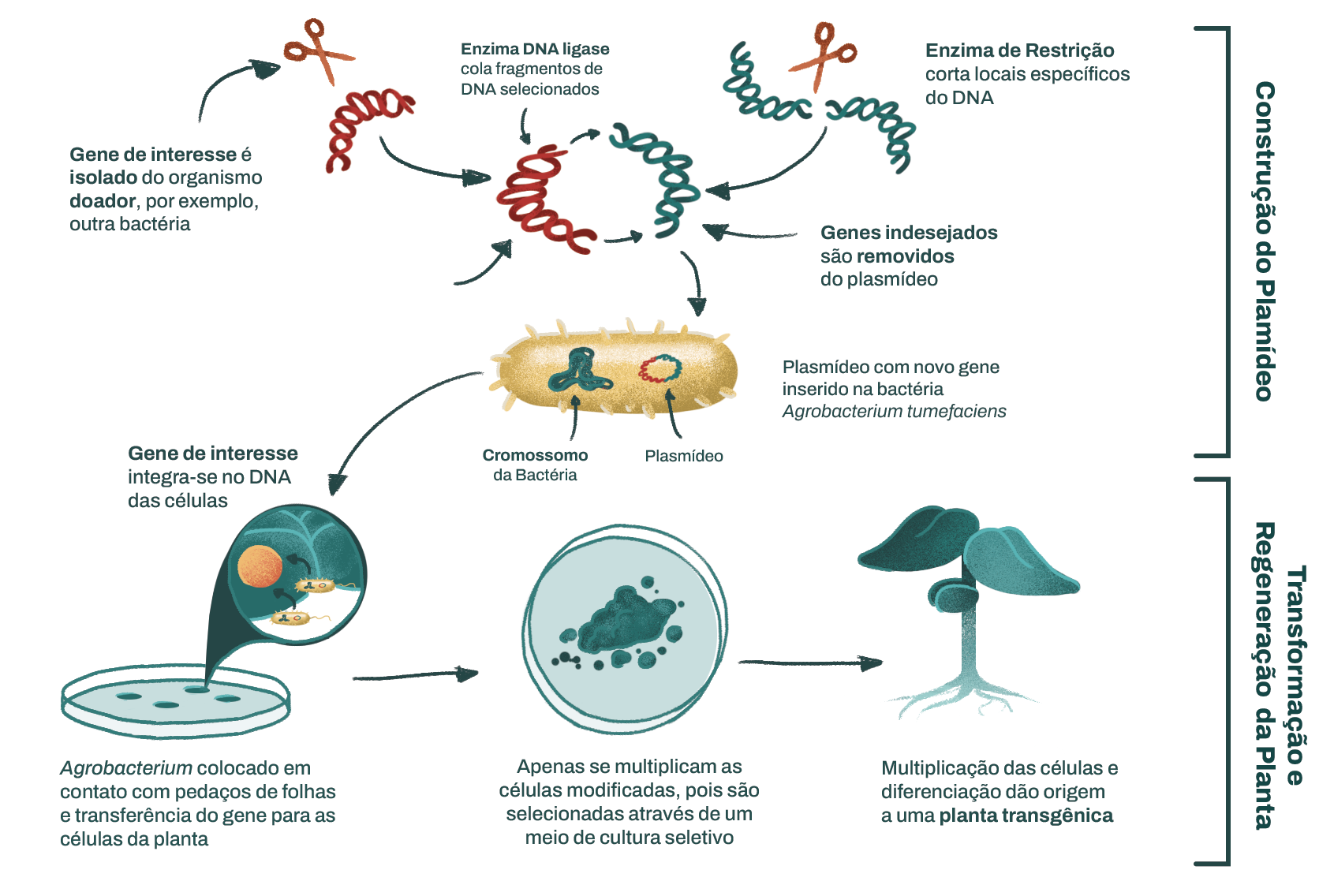
Atualmente, a maioria dos produtos transgênicos comerciais envolve a resistência às pragas, visto que elas são parte integrante da economia agrícola. Como exemplo disso, a soja e o algodão foram modificados para resistir aos efeitos do herbicida glifosato, de modo que esse possa ser aplicado para controlar as ervas daninhas após o plantio. Com isso pode-se reduzir expressivamente a quantidade de herbicida necessária. Outras combinações de herbicidas e plantas resistentes a eles estão disponíveis no mercado.
A resistência a insetos foi outra das proezas da modificação genética. Por meio da recombinação dos genes das toxinas, as plantas passaram a produzir o próprio inseticida natural. Dessa forma é possível reduzir, ou até mesmo eliminar o uso de agrotóxicos sintéticos.
Uma aplicação importante da tecnologia transgênica é a proteção contra vírus vegetais e bactérias patogênicas, que regularmente infestam e dizimam as plantações. Descobriu-se que a resistência aos vírus pode ser induzida pela incorporação de fragmentos de códigos genéticos das proteínas virais ou bactérias no genoma da planta, em um processo semelhante à vacinação. Aparentemente, os genes estranhos ativam o mecanismo de defesa da planta, que destrói o material genético do organismo invasor.
Além da proteção à planta, a engenharia genética pode produzir melhorias nessa, por exemplo, milho ou canola com maior teor de óleo, ou tomates que resistem mais ao armazenamento. Isso só é possível com a alteração genética do metabolismo vegetal.
Porém, como mencionamos anteriormente, alguns mercados mundiais, como o Japão, rejeitam fortemente a entrada de alimentos com essas características, enquanto que outros, como os norte e sul-americanos e o asiático têm aceitado essas variedades agronômicas. Fatos como esse fazem com que exista um debate bastante intenso relacionado à inserção de alimentos geneticamente modificados no mercado mundial. Desde 2004, após seis anos de proibição, a União Europeia autorizou a importação de produtos transgênicos. Somente em 2010, aprovou o plantio de batata e milho transgênicos no continente, após solicitações dos Estados Unidos. Contudo, a batata transgênica foi destinada para a fabricação de papel, adesivos e têxteis, já o milho atendeu à indústria alimentícia.
Uma das preocupações manifestadas em relação à utilização de plantas transgênicas é a possível polinização cruzada entre essas espécies com as existentes na natureza ou com culturas não modificadas. Vários estudos têm demonstrado que a existência de polinização cruzada é real, e que está diretamente relacionada ao uso de culturas transgênicas. Além disso, várias informações contraditórias têm sido lançadas por diversos setores quanto aos potenciais danos que os organismos transgênicos possam provocar nos seus consumidores. Algumas das críticas que os transgénicos têm recebido relacionam-se com a potencial reação alérgica dos animais/humanos a esses alimentos. Por fim, grande parte das polêmicas originadas com a questão dos transgênicos está diretamente relacionada a seu efeito na economia mundial, isso porque países atualmente bem estabelecidos economicamente e que tiveram sua economia baseada nos avanços da chamada genética clássica são contra as inovações tecnológicas dos transgênicos.
Construindo e fixando o conhecimento
1. Qual a importância dos ciclos biogeoquímicos para a biosfera?
2. Por que os solos cultivados devem passar por um processo de rotação de culturas?
3. No que se baseia o mecanismo de atuação dos pesticidas?
4. Por que os inseticidas naturais deixaram de ser empregados no controle de pragas?
5. Por que o DDT foi considerado durante muito tempo como um inseticida ideal?
6. Explique como ocorre o ganho de resistência ao DDT por parte dos insetos.
7. O que é a biorremediação?
8. Como atuam os inseticidas organofosforados e carbamatos?
9. Apresente o mecanismo de toxicidade do paraquat.
10. Quais são as principais vantagens do glifosato em relação aos demais pesticidas?
11. Em sua opinião, quais são as principais vantagens e desvantagens do uso de alimentos transgênicos?
Referências
BAIRD, C.; CANN, M. Química Ambiental. 4a edição. Porto Alegre: Bookman, 2011.
SPIRO, T. G.; STIGLIANI, W. M. Química Ambiental. 2a edição. São Paulo: Pearson Pretice Hall, 2009.
ROCHA, J. C.; ROSA, A. H.; CARDOSO, A. A. Introdução à Química Ambiental. 2a edição. Porto Alegre: Bookman, 2009.